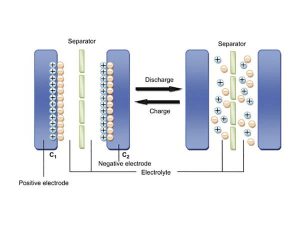
碳酸亚丙酯(PC)作为锂离子电池电解质溶剂,具有价格低廉、熔点低(-49.2°C)、介电常数高、化学稳定性高、闪点和沸点高、电化学窗口宽等优点。PC基电解液具有良好的低温和高温性能,有助于提高锂离子电池的低温性能和安全性能。然而,当PC基电解质与商业锂离子电池中广泛使用的石墨阳极材料结合使用时,PC分子将与溶剂化的锂离子一起嵌入石墨层中,并在其中发生剧烈的还原和分解反应,如图1所示,导致石墨薄片剥落并破坏石墨电极结构。
解决这一问题的有效方法是在电解质中添加成膜添加剂,它优先于PC的分解(或比PC更容易分解),并在石墨阳极材料表面形成有效、致密和稳定的SEI膜,以防止PC和溶剂化锂离子的共嵌入。因此,使用添加剂来提高PC基电解质的循环稳定性的基本原理是,添加剂必须在锂离子插入石墨电极的电势以上分解,并在石墨表面形成均匀、致密和稳定的SEI膜。这样,当放电电压降至锂嵌入电位时,可以避免由PC的共嵌入和PC的还原引起的石墨碳的分层剥离、粉化和脱落。
丁酸乙烯基(VB)、己酸乙烯基、苯甲酸乙烯基、巴豆酸乙烯基和新戊酸乙烯基(新戊酸乙烯基)可用作PC和液体电解质系统的添加剂。在PC基电解质中加入丁酸乙烯酯可以显著抑制电解质在石墨电极上的分解,提高电池的电化学性能。计算表明,VB的最低未占分子轨道(LUMO)能量与添加剂的还原势基本呈线性关系。为了在锂离子电池中常用的三种石墨碳(天然石墨、MCMB 6-28和MCF)中测试乙酸乙烯酯、己二酸二乙烯酯和碳酸烯丙酯作为PC基电解质添加剂的作用,并评估这些溶剂的直接两电子还原的可行性,以及评估这些溶剂直接两电子减少的可行性,未发现当通过VEC的分解产生Li2CO3和1,4-丁二烯(1,4-丁烯)时存在能垒。相反,EC或PC的分解需要穿过0.5eV的能垒。VEC的还原分解容易产生Li2CO3,这可以解释为什么VEC可以用作锂离子电池的钝化剂。
使用相同体积的氟代碳酸亚乙酯(氟EC)和共溶剂电解质,在石墨的第一次锂嵌入过程中电解质分解引起的容量损失降低到85mA·h/g。在含有等体积EC和PC的三元溶剂体系中,碳酸氟乙烯酯的体积分数可以进一步降低到0.05。使用含氟碳酸亚乙酯、PC和EC溶剂的电解质的锂离子电池具有长的循环寿命。经过200次循环后,电池容量减少到原来的37%,电池的电流效率为100%。因此,解决了当使用氯代碳酸乙烯酯(氯代EC)代替氟代碳酸乙烯时电池的低电流效率的问题。
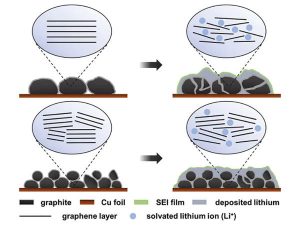
采用湿化学方法在低覆盖率的石墨化中间相碳微珠(MCMB)上沉积纳米银颗粒,发现纳米银颗粒的沉积促进了使用PC基电解质在碳电极上形成稳定的SEI膜。结果,锂离子的嵌入和脱嵌变得可逆。
碳酸亚乙烯酯(VC)可用作高反应性成膜添加剂,以最大限度地减少电解质的分解,并提高钾离子电池的充放电效率和循环特性。但VC是一种极不稳定的化合物。乙烯基碳酸亚乙酯(VEC)的分子结构与VC非常相似,但由于VEC中的双键直接连接到环外的电源基团CH,双键上的电子云密度增加,有利于稳定双键。VC中的双键直接连接到环中的吸电子基团OCOO,这降低了双键上的电子云密度,导致双键极不稳定,容易聚合。
当用作溶剂时,VEC具有高介电常数,并且具有高沸点和闪点,这有利于提高锂离子电池的安全性。对VEC作为PC基电解质成膜添加剂的物理电化学性能、还原分解机理和电化学行为以及在不同石墨形态和充放电电流密度下的电化学行为进行了详细的实验和理论研究,研究发现,VEC在1.35V时开始分解,其产物可以在片状石墨上形成致密稳定的SEI膜,可以有效防止PC和溶剂化锂离子在石墨层之间的共嵌入。VEC具有高氧化电位,并且与正极材料LiMn2O4具有良好的相容性。FTIR、XPS和GC-MS研究结果表明,VEC的主要还原产物为烷氧基锂ROLi(R为烷基)、烷基酯锂ROCO2Li、碳酸锂、锂碳化合物和1,3-丁二烯等,LiO2COCH2CH(CH=CH2)OCO2Li、LiO2COH2CH(CH=CH2)和LiCH(CH=CH2)CH2OCO2Li等等。
石墨电极在PC/VEC电解质中的电化学行为在很大程度上取决于石墨的形态和充放电电流密度。在低电流密度下,VEC的还原和分解产物可以在片状石墨表面形成有效、充分和稳定的SEI膜,但不能在球形石墨MCMB表面形成有效和充分的SEI薄膜。只有在高电流密度下,VEC的还原和分解产物才能在片状石墨和球形石墨MCMB表面形成有效且充分的SEI膜。通过简单地控制充电和放电电流密度,可以显著抑制PC和溶剂化锂离子共嵌入球形MCMB中。VEC在低电流密度下还原分解的主要产物是长链烷基酯锂LiOROCO2Li,而在高电流密度下的还原分解主要产物是无机Li2CO3。正是这种特定的还原和分解产物决定了不同形态石墨材料的不同电化学行为。
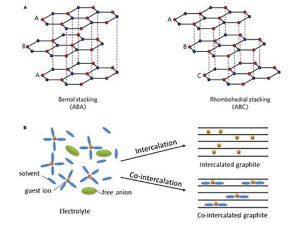
共插层涉及溶剂化离子的插入
(A) 石墨结构示意图;(B) 电解质、插层石墨和共插层石墨中配位结构的示意图。
尽管PC具有许多优点,添加少量合适的成膜添加剂可以解决其与石墨阳极材料的兼容性,但如果将其应用于实际的锂离子电池,仍有许多问题亟待解决。首先是PC的粘度过高,直接导致电解质体系的电导率[(2~6)×10-3S/cm]低于目前常用的电解质体系[(10~18)×10-3S/cm]。虽然PC基电解质的电导率可以满足普通锂离子电池的要求,但如果用于动力型锂离子电池,其电导率仍然较低;此外,PC基电解质与电极材料的渗透性非常差,因此活性材料的利用率不高。
尽管可以在PC基电解质中加入一些低沸点链碳酸酯,如DMC、DEC、EMC等,以提高系统的低温性能,提出了两种有助于解决这一问题的想法:一种是在PC基电解质中加入少量合适的表面活性剂,以降低电解质的表面张力,增加电解质和电极表面的渗透程度;二是将PC基电解质制备成类似于“啤酒”的系统,向PC基电解质中添加一些气体,并要求压力保持在电池的可接受范围内。
气体最好选择中性气体,例如CO2(PC可以吸收大量的CO2,通常使用PC来净化CO2)。该电解质体系可能具有以下优点:①在PC基电解质中加入极少量的CO2,可以显著改善石墨阳极材料表面的SEI膜,防止PC和溶剂化锂离子在石墨层之间的共嵌入;②它可以改善电解质和电极表面的渗透状态;③它可以抑制产生气体的副反应;④可以提高锂离子电池的安全性能;⑤它可能具有更高的导电性等。